
CHROMATOGRAFIA TUSZU
FLAMASTRÓW, BARWNIKÓW LIŚCI
CHROMATOGRAFICZNA KONTROLA PRZEBIEGU
SYNTEZY
**ostatnia aktualizacja: 26.03.2002**
1905-2005: STO LAT OD WYNALAZKU CHROMATOGRAFII !
W większości technik analiz jakościowych, obecność składnika obserwuje się pośrednio - w postaci innych związków, w które ten składnik przeprowadzono. W technikach ilościowych odczyt jest jeszcze bardziej abstrakcyjny. O ilości składnika informuje nas np. objętość zużytego odczynnika lub wręcz wychylenie strzałki miernika.
W wielu technikach chromatograficznych składniki mieszaniny po ich rozdzieleniu często da się obserwować w pierwotnej, niezmienionej postaci. Również o ich względnej zawartości można wnioskować bezpośrednio na podstawie intensywności/powierzchni plam. Można po prostu pokazać palcem na chromatogram: "o, właśnie to jest wykrywana substancja!". Z tego punktu widzenia chromatografia jest najwspanialszą techniką analityczną... Piękny film: http://www.youtube.com/watch?v=gzp2S0e9o8s
Niektórzy Wykładowcy omawianie chromatografii uważają za właściwe rozpoczynać od napisania Równania Izotermy Adsorpcji. Ja jednak...
Jako ilustrację proponuję chromatografię cienkowarstwową tuszów flamastrów na żelu krzemionkowym. Plamy startowe nanoszono po prostu przez dotknięcie końcówką pisaka do płytki w miejscach oznaczonych numerami. Zaznaczono również miejsce do którego dotarł "front" rozpuszczalników. Najbardziej zaskakujące wyniki daje analiza czarnego tuszu (1). Producent sporządził go z mieszaniny aż czterech barwników, które po zmieszaniu dają wrażenie neutralnej czerni; tusz brązowy został sporządzony z takiej samej mieszaniny, w której zastosowano jedynie nieco inne proporcje. Na załączonym zdjęciu (poprawnie powinno ono być w położeniu pionowym) wygląd plam ostatnich dwóch tuszów fluoryzujących został wyraźnie zafałszowany z powodu nieprzystosowania charakterystyki czułości elementu czytnika skanera do efektu fluorescencji tuszu. Porównawcza analiza chromatograficzna tuszów i atramentów jest czasem wykorzystywana praktycznie - do ujawnienia fałszowania dokumentów np. bankowych.

Chromatografia
cienkowarstwowa tuszu flamastrów "Sanford" na żelu
krzemionkowym Merck
w układzie: octan etylu+etanol+woda 5+3+2
(objętościowo)
1 czarny |
2 brązowy |
3 niebieski |
|
4 zielony |
5 fioletowy |
6 żółty |
|
7 czerwony |
8 żółty fluoryzujący | 9 pomarańczowy fluoryzujący |
|
chromatografia czarnych flamastrów
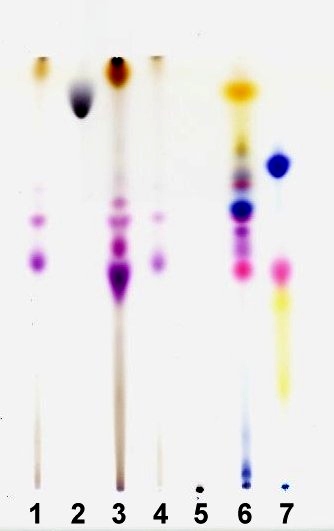
Obok przedstawiam chromatogram próbek tuszów siedmiu różnych flamastrów. Patrząc na to zdjęcie nikt nie domyśliłby się, że wszystkie te flamastry były koloru czarnego! Oryginalny jest wynik analizy tuszu 2; składa się on bowiem tylko z jednego składnika; producent zadał sobie sporo trudu w zdobyciu takiego właśnie czarnego barwnika... Trudno jest z całą pewnością stwierdzić to samo o próbce 5; warunki analizy nie są odpowiednie do ewentualnego rozdzielenia substancji o tak małych wartościach Rf. Być może tusz 5 po prostu zawiera sadzę. Z kolei próbka 6 składa się z ponad 10 barwników. Natomiast składy tuszów próbek 1 i 4 (i ewentualnie 3) są bardzo do siebie podobne. Przypuszczam, że na podstawie tych chromatogramów Czytelnik mógłby podjąć się ekspertyzy dotyczącej fałszerstwa podpisu.
Z chromatografią tuszu flamastrów miałem kiedyś mało sympatyczną przygodę. Podczas rutynowej kontroli w pociągu, Rewizorka wsadziła moją legitymację do torby oświadczając, że wpis przedłużający ważność jest sfałszowany! Wpis dokonany był właśnie flamastrem, a legitymacja noszona w kieszeni wystawiona była na wilgoć i ciepło. Oczywiście zaszła częściowo chromatografia, a jej wynik widoczny był w postaci wielobarwnych obwódek wokoło wpisu. Trwające wiele miesięcy handryczenie się z urzędami przerwałem wreszcie żądając, aby PKP wystąpiły wobec mnie na drogę sądową o fałszerstwo...
zastosowanie chromatografii cienkowarstwowej do kontroli przebiegu reakcji
Przeprowadzono reakcję estryfikacji aminokwasu:
NH2[---]COOH ® TosOH NH2[---]COOC7H7
Symbolem: [---] oznaczono środkowy fragment cząsteczki aminokwasu (tu: L-fenyloalanina), a TosOH oznacza kwas p-toluenosulfonowy (żargonowo: "tozylowy"); w postaci takiej soli estry aminokwasów są trwałe, a prócz tego tozylany są łatwe do krystalizacji. Wzory substancji kwasowych zaznaczono kolorem czerwonym, a zasadowych - niebieskim. Szczegóły przebiegu syntezy estrów benzylowych aminokwasów można znaleźć w jakiejkolwiek preparatyce organicznej.
W wyniku dwudniowej pracy, z białego proszku (wyjściowy aminokwas) otrzymano biały proszek (?).
Należy ustalić:
czy otrzymany produkt jest istotnie pochodną aminokwasu, czy też jest to niezmieniony (nieprzereagowany) substrat?
czy produkt jest zanieczyszczony domieszką substratu (i ewentualnie w jakim stopniu)?
jaka jest skuteczność oczyszczania otrzymanego estru?
Przy oczyszczaniu wykorzystać można różnice właściwości kwasowych substratu i produktu (ester nie jest kwasem).
aminokwas |
ester aminokwasu |
||
rozpuszczalność w eterze |
NIE |
TAK |
|
rozpuszczalność roztworze Na2CO3 |
TAK |
NIE |
|
Surowy produkt rozpuszczony w rozcieńczonym roztworze Na2CO3 i wstrząsany z eterem (rozpuszczalnik ten nie miesza się z wodą), ulega ekstrakcji do eteru. Ewentualne zanieczyszczenie wolnym aminokwasem pozostaje w roztworze wodnym w postaci rozpuszczalnej w wodzie soli aminokwasu.
2 NH2[---]COOH
+ Na2CO3
® 2 NH2[---]COO–
Na+
+ CO2 + H2O
2 TosOH NH2[---]COOC7H7
+ Na2CO3
® 2 TosONa
+ 2 NH2[---]COOC7H7
+ CO2 + H2O
Sporządzić w mikroprobówkach roztwory:
A substrat: aminokwas w wodzie (ok. 1 mg fenyloalaniny w jednej kropli, na ciepło)
B surowy produkt - w etanolu (kilka mg w jednej kropli)
C w probówce umieścić nieco surowego produktu, dodać kilkanaście kropel roztworu Na2CO3 oraz ok. 1 ml eteru. Wstrząsnąć. Do analizy pobrać kapilarą roztwór eterowy (górny). Dla zwiększenia czułości testu, na płytkę naniesiono znacznie więcej tego roztworu, niż roztworu B
Na płytkę chromatograficzną pokrytą żelem
krzemionkowym nanieść za pomocą kapilary szklanej trzy plamki - jak na
rysunku. Kapilara ma grubość włosa końskiego; jedna kropla roztworu
wystarcza do wykonania kilkudziesięciu chromatogramów. Chromatogram rozwijać w układzie: chloroform+metanol+woda
amoniakalna 10+1+0,1 (objętościowo). Natychmiast po wyjęciu płytki z
komory zaznaczyć na niej ołówkiem front rozpuszczalników. Po naniesieniu
plamek roztworów i po zakończeniu chromatografii, na płytce nie widać oczywiście
żadnej z bezbarwnych substancji. Płytkę
starannie wysuszyć 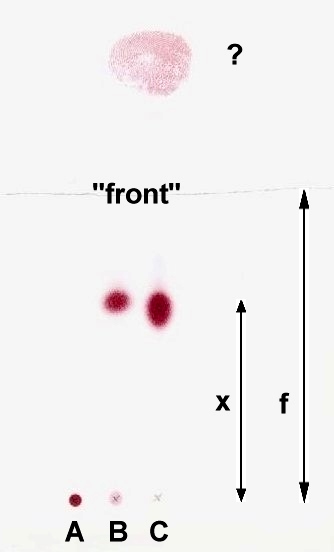 (konieczne jest usunięcie śladów amoniaku), następnie spryskać
1-procentowym roztworem ninhydryny
w etanolu i ogrzać przez kilka minut do temp. ok. 60 0C. Ninhydryna daje zarówno
z wolnymi aminokwasami, jak i ich estrami różowofioletowe zabarwienie.
Zmierzyć linijką wartości Rf (ratio of front = "w
proporcji do dystansu przebytego przez front"). Jest to wielkość
liczbowa charakterystyczna dla substancji podobnie, jak np. jej temperatura
topnienia.
(konieczne jest usunięcie śladów amoniaku), następnie spryskać
1-procentowym roztworem ninhydryny
w etanolu i ogrzać przez kilka minut do temp. ok. 60 0C. Ninhydryna daje zarówno
z wolnymi aminokwasami, jak i ich estrami różowofioletowe zabarwienie.
Zmierzyć linijką wartości Rf (ratio of front = "w
proporcji do dystansu przebytego przez front"). Jest to wielkość
liczbowa charakterystyczna dla substancji podobnie, jak np. jej temperatura
topnienia.
Na podstawie obrazu wywołanego chromatogramu można orzec, że:
- otrzymany biały produkt jest rzeczywiście pochodną aminokwasu (reaguje z ninhydryną, a jednocześnie jest to inna substancja, niż wyjściowy aminokwas)
- produkt jest zanieczyszczony wyjściowym aminokwasem (dwie plamy = dwie substancje). Produkt jest zanieczyszczony substratem w niewielkim tylko stopniu (mała intensywność plamy substratu w miejscu startu)
- zastosowana metoda oczyszczania estru (ekstrakcja z zasadowego roztworu wodnego - do eteru) jest skuteczna: po ekstrakcji brak jest śladów zanieczyszczenia, i to pomimo naniesienia bardzo znacznej ilości substancji
- trochę dla żartu, na płytce ponad chromatogramem naniesiono odcisk ("?") palca zwilżonego śliną. Intensywnie barwna plama linii papilarnych jest dowodem czułości reakcji z ninhydryną.
Z czułością detekcji wiąże się kolejna anegdota. Na Północy Kanady zaobserwowano podczas tarła łososi, że wejście niedźwiedzia (zapamiętale polującego właśnie na łososie) do wody, powoduje po krótkim czasie paniczny popłoch wśród ryb znajdujących się nawet 100 m niżej w strumieniu. Okazało się, że czynnikiem alarmowym jest aminokwas seryna zawarta w pocie łapy niedźwiedzia. Po jego wejściu do wody seryna rozpuszcza się w wodzie i unoszona prądem wody jest powodem alarmu ryb... Można ocenić, jak niewiele cząsteczek seryny dociera do receptora łososia! (czułość: 10-11 g/ml). Nieco podobny monitoring jest stosowany praktycznie do kontroli czystości wody wychodzącej z oczyszczalni ścieków. Wszystko to jednak nie daje się porównać z czułością motyli. Reagują one z odległości kilometra na pojedyncze cząsteczki substancji wabiących (F feromony)...
Wartość Rf estru benzylowego fenyloalaniny wynosi: Rf = x : f = 50 mm : 78 mm = 0,64. Wartość Rf wolnego aminokwasu równa jest w tych warunkach praktycznie zero (podczas chromatografii w tych warunkach pozostaje on na starcie). Podając wartości Rf trzeba jednocześnie opisywać warunki rozdziału (przede wszystkim rodzaj nośnika oraz skład fazy ruchomej). Ilość składnika jest (w dużym przybliżeniu) proporcjonalna do powierzchni plamy.
W tym miejscu trzeba wyraźnie zaznaczyć, że chromatogramy tak piękne jak powyższy, są w chemicznej praktyce raczej rzadkością. Z reguły plamy są mniej lub bardziej rozciągnięte, a często plamy substancji zachodzą na siebie; utrudnia to oczywiście interpretację wyników. Takie właśnie koszmarnie rozmyte chromatogramy śnią się czasem chemikom po nocach... Oraz to, że w nocy zaciął się kolektor frakcji i roztwór cennej substancji znajduje się na podłodze.
chromatografia barwników liści
Chromatografię wynalazł rosyjski chemik M.Cwiet w 1905 r. w Warszawie (był to wtedy uniwersytet rosyjski). Pierwszymi rozdzielonymi mieszaninami były barwniki roślin; właśnie z powodu barwności plam poszczególnych składników metoda została nazwana chromatografią.
Nomen-omen: przypadkowo podobne znaczenie ma nazwisko odkrywcy; "cwiet" po rosyjsku znaczy: "barwa".

Do powyższej analizy użyto chloroformowego ekstraktu liści trawy roztartej w moździerzu; układ rozwijający: cykloheksan + aceton 4+1,5 (objętościowo). Plamy, które na chromatogramie oznaczone są jako "x", w świetle lampy UV intensywnie fluoryzują różowo; zawierają więc chlorofil. Co prawda w roślinach znajduje się zasadniczo tylko chlorofil a i chlorofil b lecz pozostałe plamy są prawdopodobnie produktami degradacji kompleksów chlorofilów z białkami. Plama ksantofilu na tym chromatogramie jest nałożona na plamę jednego z chlorofilów.
Inne proponowane układy rozpuszczalników
eter naftowy 60%, cykloheksan 16%, octan etylu 10%, aceton 10%, metanol 4%.
cykloheksan 59%, aceton 25%, eter 25% .
Wbrew potocznemu przekonaniu, chlorofil wcale nie jest tak zupełnie zielony; barwa jednej jego odmiany jest szaroniebieskawa, a drugiej: niebieskozielona (natomiast chloroformowy oliwkowozielony ekstrakt liści, w świetle UV fluoryzuje wiśniowo!). Zielony kolor liści powstaje z nałożenia pozostałych barwników: karotenoidów (na chromatogramie są to plamy o największej wartości Rf) i ksantofilu, a czasem dodatkowo antocyjanów. Malownicze zmiany barwy liści jesienią powodowane są przez stopniowy zanik poszczególnych barwników (pierwszy zanika chlorofil). Różowa fluorescencja chlorofilu daje się obserwować dopiero po ekstrakcji lub innym uszkodzeniu komórek. Wykorzystywane jest to do lokalizacji obszarów Ziemi, na których szata roślinna jest uszkodzona mechanicznie lub biologicznie. Na zdjęciach satelitarnych takich miejsc wyraźnie widoczna jest fluorescencja chlorofilu.
**
Satelita ORBVIEW z instrumentem SeaWiFS na pokładzie pomaga między innymi w określaniu globalnych i lokalnych koncentracji chlorofilu w wodach oceanów. Dzięki satelicie naukowcy mogą monitorować ocean w skalach od 3 dni do tygodni, miesięcy i lat. Prezentowana fotografia jest jednym z pierwszych takich pomiarów wykonanych przy pomocy SeaWiFS. Prezentuje średnią koncentrację barwnika we wrześniu 1997 roku. Dane były poddawane trzykrotnej obróbce komputerowej.
[zdjęcie i tekst zaczerpnięty z: http://gallery.astronet.pl/index.cgi?116 . Warto wejść: są tam inne wspaniałe zdjęcia! oraz stronę: http://visibleearth.nasa.gov/cgi-bin/viewrecord?7647 ] **
o metodzie
W każdej technice chromatograficznej istnieją podobne stałe elementy.
W przypadku substancji bezbarwnych, po rozdziale używa się odczynników dających barwne produkty z poszczególnymi składnikami. Daje to często możliwość jakościowej identyfikacji składników. Stosowane są np. wskaźniki pH (kwasy lub zasady), roztwór KI + skrobia (utleniacze), mieszanina FeCl3 + K3Fe(CN)6 (reduktory) oraz odczynniki specyficzne (do poprzedniego chromatogramu użyto ninhydryny - odczynnika specyficznego dla aminokwasów). Uniwersalne metody lokalizacji plam: oglądanie chromatogramu w świetle lampy UV (niektóre substancje fluoryzują, inne widoczne są na tle fluoryzującego podłoża), ogrzanie po spryskaniu roztworem kwasu siarkowego (zwęglanie większości substancji organicznych), adsorpcja par jodu (powstają brunatne plamy stałego roztworu jodu lub kompleksów charge-transfer z jodem).
W technikach kolumnowych poszczególne składniki opuszczają kolumnę kolejno, w różnym czasie. Ich pojawianie się można śledzić mierząc wartość ekstynkcji roztworu (często jest to pomiar w zakresie UV). Chromatogram ma wtedy postać wykresu zależności ekstynkcji jako funkcji czasu (dokładniej: objętości wycieku).
Chromatografia jest techniką zarówno analityczną, jak i preparatywną (nawet na skalę przemysłową). Jeśli ktoś chciałby wyodrębnić np. poszczególne składniki tuszu, może zdrapać odpowiednie plamy wraz z nośnikiem, i wyługować zaadsorbowany składnik.
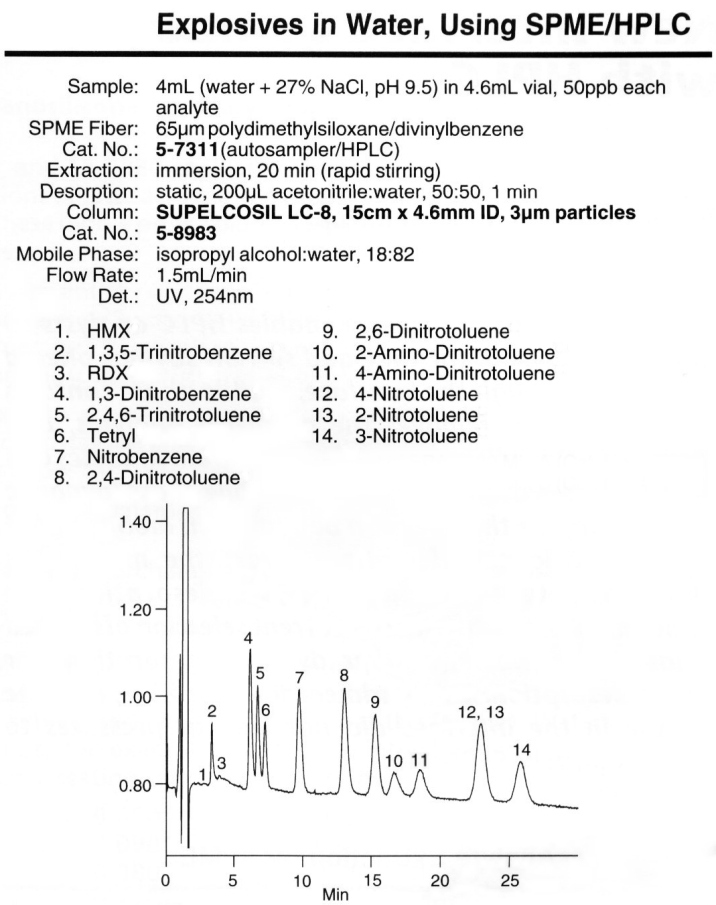
Postęp w technologii urządzeń (nośnik, pompy, detekcja, rejestracja, komputerowe sterowanie i numeryczna obróbka wyników) w Wysokosprawnej Chromatografii Cieczowej HPLC pozwala na dokonanie (powtarzalnego!) rozdziału próbek o masie rzędu milionowych części grama, ich identyfikacji i oznaczenie liczbowe zawartości (ilość składnika jest proporcjonalna do całki pod pikiem ekstynkcji). Jest zrozumiałe, że koszt zestawu do HPLC jest rzędu ceny dobrego samochodu... Ilustracją niech będzie zaczerpnięty z prospektu reklamowego wynik analizy (metodą HPLC połączonej z ekstrakcją) próbki wody odpadowej po produkcji materiałów wybuchowych. Stężenie 50 ppb = 1 g substancji w 20 m3 wody ! Aby ustalić rodzaj produkcji wcale nie trzeba było wynajmować J.Bonda, który na terenie zakładu nocą ukradkiem pobierał próbki. Wystarczyło z rzeki poniżej odprowadzenia ścieków poprodukcyjnych pobrać próbki wody...
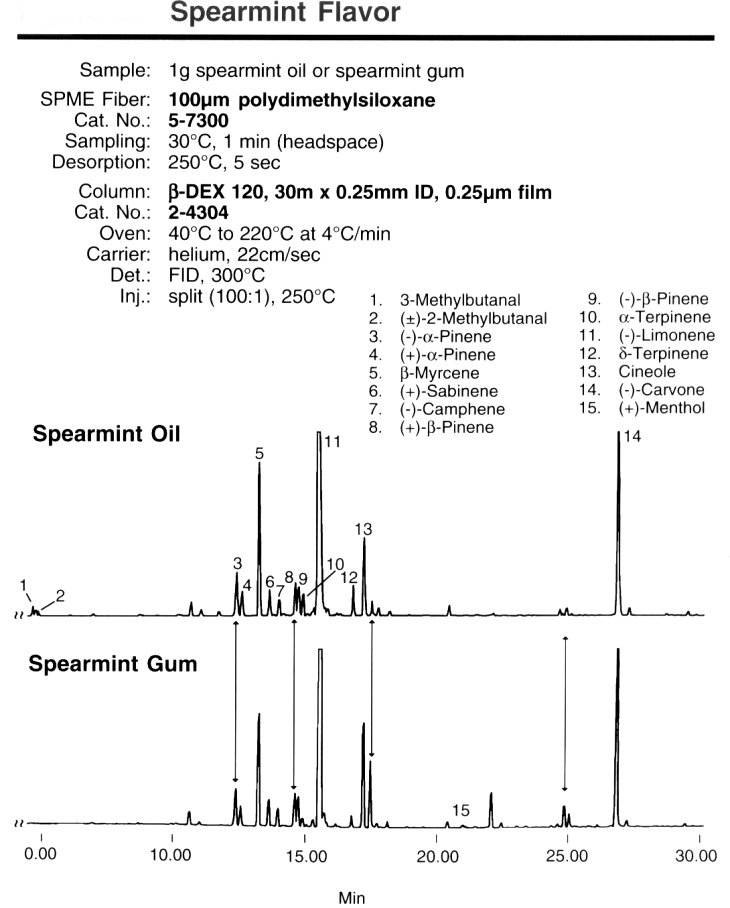
oraz wynik chromatografii gazowej środków aromatyzujących miętowej gumy do żucia
LITERATURA
T.Pluciński. "Doświadczenia chemiczne" . Wyd. “Adamantan”, Warszawa 1997, s. 119.
[Chromatografia tuszu flamastrów i barwników liści]
J.Chem.Educ. 79, 922 (2002) [Historia chromatografii]
J.Chem.Educ., 81, 385 (2004). [Usprawniona TLC barwników liści]
Kurier Chemiczny
J.Chem.Educ. 73, 306 (1996). [Antocyjany,
analiza chromatograficzna]
J.Chem.Educ., 43, A124 (1996). [Synteza soli flawyliowej]
S.Zalewski (redaktor), “Technologia przyrządzania potraw”, Wyd. SGGW-AR,
Warszawa 1978, s. 78. [Zmiany barwy owoców i warzyw podczas przygotowywania
potraw]
http://photoscience.la.asu.edu/photosyn/education/colorchange.html
http://www.esf.edu/pubprog/brochure/leaves/leaves.htm
zmiany barw liści jesienią
http://gallery.astronet.pl/index.cgi?116
galeria astro-zdjęć
Tomasz Pluciński
nowy adres:
tomasz.plucinski@ug.edu.pl
| F | strona główna |