NIEZWYKŁE
EKSPERYMENTY Z NIEZWYKŁYM TLENEM
dawno
temu...
Skroplenie
tzw. gazów
trwałych, m.in. tlenu - było przed laty prawdziwym wyzwaniem
technicznym oraz sensacją. Dokonano tego żmudną metodą kaskadową. Chłodząc
sprężone pary łatwo skraplającego się gazu, a następnie gwałtownie
odparowując otrzymaną ciecz - uzyskiwano spadek temperatury aż o kilkadziesiąt
stopni. W tych warunkach skraplano kolejny, trudniej skraplający się czynnik
gazowy. Po wielu takich żmudnych operacjach osiągnięto temperaturę w której
zaczynał skraplać się najmniej lotny składnik powietrza - tlen. Tak postąpili
w 1883 roku Olszewski i Wróblewski.
dziś...
Dziś
stosowana jest niemal wyłącznie metoda rozprężania wykorzystująca tzw.
efekt Joule'a-Thomsona. Oczyszczone suche powietrze spręża się do wysokiego ciśnienia
i otrzymany bardzo gorący, silnie sprężony gaz - chłodzi wodą. Powietrze
jest następnie rozprężane przez zawór dławiący; towarzyszy temu znaczne
obniżenie temperatury. Oziębiony rozprężony gaz przechodzi przez wymiennik
ciepła ochładzając dopływający stale do zaworu dławiącego gaz
pod wysokim ciśnieniem. W wyniku kolejnych wymian ciepła temperatura
rozprężanego powietrza ciągle spada, aż rozpoczyna się jego skraplanie...
W praktyce produkcja azotu i tlenu odbywa się w sposób ciągły,
poprzez odbieranie odpowiednich frakcji z kolumny rektyfikacyjnej znajdującej
się za strefą rozprężania. Koszty produkcji obejmują jedynie cenę energii
elektrycznej sprężarki oraz eksploatacji urządzeń i koszta administracyjne.
Skraplanie
wodoru np. do instalacji zasilającej kosmiczne urządzenia startowe jest
bardziej kłopotliwe, gdyż wodór w zwykłej temperaturze ma odwrotny znak współczynnika
Joule'a-Thomsona (podczas rozprężania wodór się ogrzewa a nie oziębia). Przed
poddaniem wodoru rozprężaniu, należy go wstępnie silnie ochłodzić w
tradycyjny sposób. To nie koniec kłopotów. Świeżo skroplony wodór jest
bardzo niestabilny z powodu dość szybkiej przemiany
F
ortowodoru
w parawodór. Co prawda
ciepło tego egzotermicznego procesu jest niewielkie, ale równie małe jest
ciepło parowania ciekłego wodoru. W rezultacie, nawet przy idealnej izolacji,
w ciągu kilkunastu godzin samorzutnie i bez dopływu ciepła z zewnątrz,
odparowuje w wyniku tego prawie połowa skroplonej cieczy. Podczas skraplania
wodoru stosuje się paramagnetyczny katalizator przyspieszający opisaną
przemianę. W ten sposób co prawda wydajność skraplania jest znacznie niższa,
ale otrzymany ciekły wodór znajduje się w stanie równowagi i jest znacznie
bardziej stabilny. Jeszcze inna ciekawostka kosmiczna dotyczy oszczędności
masy zbiorników paliwa rakiety (w przypadku Space Shuttle jest to ten największy element zestawu startowego).
Buduje się go z bardzo cienkiej blachy; tak cienkiej, że załamałaby się
podczas przeciążeń startowych. Zbiornik jest stale otwarty, gdyż skroplony
wodór stale w nim wrze. Kilkadziesiąt sekund przed startem zamyka się jednak
zawór wylotowy (pressurization
has began...); rosnące ciśnienie wewnątrz usztywnia konstrukcję
podobnie jak zamkniętą puszkę z piwem...
atrakcyjne
ale
żmudne doświadczenie
Obrót
ciekłym tlenem, a nawet ciekłym powietrzem jest utrudniony z powodu przepisów
związanych z zagrożeniem pożarowym. Ponieważ doświadczenia z ciekłym
tlenem są równie atrakcyjne jak i pouczające, nie pozostawało mi nic innego
jak skraplanie go wobec audytorium. Pożyteczne będzie tu przytoczenie
temperatur wrzenia kilku
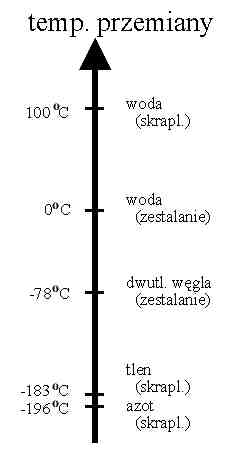 interesujących substancji. Ponieważ jednak powoduje
to odwieczny problem dydaktyczny: która temperatura jest wyższa: -183 o
C czy -196 o C, zatem proponuję posłużenie się osią liczbową.
Dodatkowo będzie widoczne, że skoro temperatura otoczenia jest o ok. 200 o
C wyższa od temperatury wrzenia ciekłego powietrza, to ciecz ta stale wrze.
interesujących substancji. Ponieważ jednak powoduje
to odwieczny problem dydaktyczny: która temperatura jest wyższa: -183 o
C czy -196 o C, zatem proponuję posłużenie się osią liczbową.
Dodatkowo będzie widoczne, że skoro temperatura otoczenia jest o ok. 200 o
C wyższa od temperatury wrzenia ciekłego powietrza, to ciecz ta stale wrze.
Ponieważ
podczas pokazów dysponuję skroplonym azotem o temperaturze ponad 10 o
C niższej, więc skroplenie tlenu jest dla mnie bez porównania łatwiejsze niż
dla Olszewskiego i Wróblewskiego. W termosie z ciekłym azotem (-196 o
C) zanurzam większą probówkę połączoną rurką w pewny sposób z balonem
(lub dętką) uprzednio napełnionym osuszonym tlenem z butli. Po chwili na dnie
probówki zaczyna gromadzić się skroplony tlen. Z reguły chcę zademonstrować
jego niebieski kolor, właściwości paramagnetyczne oraz reaktywność chemiczną.
Niestety, z reguły otrzymana ciecz jest zanieczyszczona bardzo łatwo zestalającymi
się zanieczyszczeniami: wodą (temp. zestalania 0 o C) i
dwutlenkiem węgla (temp. resublimacji : -78 o C).
genialnie
proste
 Na
pokazach fizycznych gdańskiego Festiwalu Nauki podpatrzyłem rozwiązanie
(demonstrowane z wielką dydaktyczną swobodą przez Pana dr Andrzeja
Kuczkowskiego z PG) które urzekło mnie swą prostotą i skutecznością! Do
demonstracji wystarczy dysponować zapasem ciekłego azotu i aluminiową puszką po piwie
(pustą). Pochyloną pod kątem puszkę umieścić w łapie statywu i ostrożnie
napełnić ją w 2/3 skroplonym azotem.
Zewnętrzne ścianki pokrywają się
szybko białym nalotem lodu i stałego dwutlenku węgla. Po chwili szron w
dolnej części naczynia „wilgotnieje”, a po kilkunastu kolejnych sekundach
z najniższego miejsca zewnętrznej krawędzi puszki zaczynają dość szybko kapać
kropelki. Jest to czysty skroplony tlen! Tlen pochodzi z otaczającego
powietrza, a zanieczyszczenia wodą i dwutlenkiem węgla pozostają w postaci
zestalonego szronu, przyczepione do powierzchni puszki. Czy można sobie
wyobrazić prostszą i bardziej elegancką procedurę?
Zwracam uwagę, że puszka koniecznie powinna być aluminiowa, a nie podobnie
wyglądająca stalowa - aluminium ma znacznie lepsze przewodnictwo cieplne.
Na
pokazach fizycznych gdańskiego Festiwalu Nauki podpatrzyłem rozwiązanie
(demonstrowane z wielką dydaktyczną swobodą przez Pana dr Andrzeja
Kuczkowskiego z PG) które urzekło mnie swą prostotą i skutecznością! Do
demonstracji wystarczy dysponować zapasem ciekłego azotu i aluminiową puszką po piwie
(pustą). Pochyloną pod kątem puszkę umieścić w łapie statywu i ostrożnie
napełnić ją w 2/3 skroplonym azotem.
Zewnętrzne ścianki pokrywają się
szybko białym nalotem lodu i stałego dwutlenku węgla. Po chwili szron w
dolnej części naczynia „wilgotnieje”, a po kilkunastu kolejnych sekundach
z najniższego miejsca zewnętrznej krawędzi puszki zaczynają dość szybko kapać
kropelki. Jest to czysty skroplony tlen! Tlen pochodzi z otaczającego
powietrza, a zanieczyszczenia wodą i dwutlenkiem węgla pozostają w postaci
zestalonego szronu, przyczepione do powierzchni puszki. Czy można sobie
wyobrazić prostszą i bardziej elegancką procedurę?
Zwracam uwagę, że puszka koniecznie powinna być aluminiowa, a nie podobnie
wyglądająca stalowa - aluminium ma znacznie lepsze przewodnictwo cieplne.
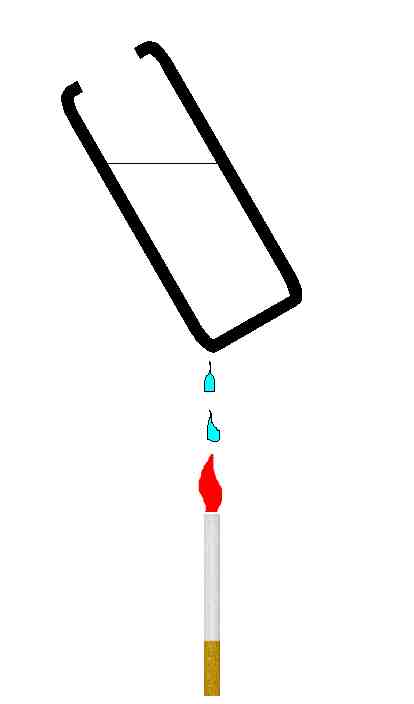
gwałtowne
spalanie
Równie
prosto można wykazać reaktywność ciekłego tlenu. Pod krawędzią puszki
przed eksperymentem umieścić postawiony pionowo na stole, zapalony papieros.
Kolejne kapiące kropelki tlenu powodują rytmiczne wybuchy płomienia. Warto
pamiętać, że stężenie skroplonego tlenu jest kilka tysięcy razy większe
niż w powietrzu. Dlatego spalanie jest tak gwałtowne.
Porowate palne materiały
nasycone ciekłym tlenem, są silnie wybuchowe. Jednymi z bezpiecznych górniczych
materiałów wybuchowych są oksylikwity.
Są to gilzy wypełnione sproszkowanym węglem aktywnym, antracenem lub innymi
palnymi substancjami. Tuż przed użyciem nasyca się je w termosie skroplonym
tlenem, dołącza spłonkę detonującą i całość umieszcza w odwiercie. W
przypadku niewybuchu wystarczy odczekać kilkadziesiąt minut. W tym czasie tlen
wyparowuje, a ładunek nie przedstawia już żadnego niebezpieczeństwa. Obecność
zaledwie 1 procenta tlenu w ciekłym azocie stwarza już pewne zagrożenie.
Operowanie ciekłym azotem w płaskim naczyniu powoduje, że w krótkim czasie
zanieczyszcza się on znacznymi ilościami tlenu. Natomiast przechowywanie
skroplonego azotu w typowym naczyniu Dewara z wąskim wlotem nie stwarza
niebezpieczeństwa pożarowego (dlaczego?).
dlaczego
są niebieskie?
Niebieski
kolor ciekłego tlenu spowodowany jest nietypową budową cząsteczki tlenu. W
zwykłym stanie, ma ona zupełnie niezwykłą budowę: zawiera dwa niesparowane
elektrony, a więc jest dwurodnikiem („stan trypletowy”). To właśnie
łatwość wzbudzenia tych niesparowanych elektronów jest powodem barwy. Tak
naprawdę, ciekły tlen jest nie tyle niebieski, ile ma lekki odcień
niebieskawy, który jest widoczny dopiero w warstwie grubszej niż 1-2 cm. Barwa na załączonym
wyżej rysunku jest znacznie przesadzona.
W tym miejscu wypada jednak
zaznaczyć, że niebieski kolor nieba nie ma z tym nic wspólnego. Kolor nieba
powodowany jest przez fizyczny efekt rozproszenia światła na niewielkich cząsteczkach
azotu i tlenu. Z kolei niebieski kolor wody, a w szczególności - lodu,
powodowany jest przez niezwykłą właściwość ciekłego i stałego tlenku
wodoru. Jest to jedyna znana substancja której pasmo oscylacyjne sięga częściowo
w zakres światła widzialnego (z reguły widma oscylacyjne położone są w
podczerwieni). Tu proponuję obejrzenie zdjęcia nieba o zachodzie słońca.
Jest o tyle niezwykłe, że wykonane zostało na Marsie przez sondę Mars
Pathfinder.

Przy okazji proponuję prostą metodę napełnienia
np. cylindra miarowego tlenem - do pokazów chemicznych. Nad wylotem cylindra
wystarczy potrzymać przez parę minut puszkę ze skroplonym azotem. Kapiące do
cylindra krople tlenu odparowują po upadku na dno i stopniowo chłodny gazowy
tlen wypełnia od dołu cylinder, wypierając z niego powietrze.
paramagnetyzm
i „lewitacja”
Substancje
zbudowane z cząsteczek mających niesparowane elektrony, są z reguły
paramagnetyczne. Znany jest eksperyment polegający na wlaniu niewielkiej ilości
ciekłego tlenu pomiędzy bieguny silnego elektromagnesu. Niektóre kropelki
pozostają „uwięzione” pomiędzy biegunami.
(Warto
zaznaczyć, że ozon jest diamagnetyczny).
Jeszcze jedna anegdota. Pewien
znany chemik, podczas wykładu, wskazując palcem
F
„wiszące”
w polu magnetycznym drgające krople tlenu, zawołał: to
właśnie jest paramagnetyzm! A nie rysowanie kredą po tablicy jakichś strzałek
i kresek! Czyż może być lepsze motto i wskazówka dla dydaktyków
nauk doświadczalnych? Rzeczywistość szkolna i uniwersytecka jest jednak zupełnie
żałosna. A ja twierdzę wręcz, że uczenie chemii bez demonstracji, wyłącznie
kredą po tablicy - jest po prostu sabotażem dydaktycznym!
Uważa
się powszechnie, że do takiego pokazu niezbędny jest ciężki silny magnes.
Można jednak posłużyć się prostym trickiem. Pod krawędź puszki podstawić
wklęsłe szkiełko zegarkowe. Tworzy się większa kropla ciekłego tlenu,
poruszająca się przypadkowo i odizolowana od szkiełka „poduszką” gazową
(podobnie zachowuje się woda nalana na silnie rozgrzaną blachę, tzw. zjawisko
Leidenfrosta).
Kiedyś próbowałem przed
nalaniem ciekłego tlenu ochłodzić silnie szkiełko zegarowe ciekłym azotem -
aby tlen dłużej pozostał ciekły. I nie udało się, bo tlen przywarł
najpierw do szkła, a w chwilę potem gwałtownie zawrzał. Okazuje się
paradoksalnie, że wytworzenie poduszki gazowej w wyższej temperaturze jest
znacznie skuteczniejsze.
Wystarczy
do takiej drgającej „lewitującej” kropli tlenu zbliżyć sztabkowy magnes
(np. zwykłe laboratoryjne mieszadełko magnetyczne przymocowane gumką do
szklanej bagietki; jeszcze lepszy może być mały magnesik samarowy lub
neodymowy).
Drgająca kropla tlenu dość wyraźnie ulega przyciągającemu wpływowi pola
magnetycznego (w przypadku magnesu neodymowego wręcz "skacze" w jego kierunku!). Być może trzeba będzie poczekać, aż kropla zmniejszy się do
optymalnych rozmiarów.

Do
demonstracji nie jest więc potrzebna ani specjalna aparatura do skraplania
gazu, ani nawet zapas tlenu, ani silny magnes!
http://www.youtube.com/watch?v=Lt4P6ctf06Q
Trzeba jednak mieć niewielką
porcję ciekłego azotu. Wbrew pozorom, nie jest to zadanie niewykonalne.
Skroplony azot używany jest np. w kriogenice medycznej (chociażby do usuwania
brodawek) jak i w zootechnice (punkty unasienniania). Jeśli doszukamy się właściwego
kontaktu wśród znajomych naszych znajomych, to pewnie możliwe będzie
zorganizowanie wizyty podczas transportu termosu ze skroplonym azotem po drodze
z wytwórni do miejsca pracy. I w taki sposób można pokazać skraplanie tlenu
nawet w niewielkiej wiejskiej szkole - jeśli się tylko chce...
Przyznam się, że przez chwilę
było mi trochę głupio, że autorzy pierwszego skroplenia musieli się tak
bardzo namęczyć, a my możemy zrobić to aż tak łatwo! No cóż: oni w
zamian zyskali sławę, a ja zamiast obiecywanej od paru lat przez Rząd podwyżki
pensji
(nie napiszę jakiej wysokości, aby nie rozbawić zbytnio Czytelników. Wcale
nie jest to takie śmieszne!) - doczekałem się podwyżki pensum godzin
dydaktycznych zafundowanej wykładowcom przez P.T. Władze mojej Uczelni. A już
teraz obiecywana solennie jest kolejna podwyżka...
Więcej o magnetyzmie:
magnetyzm.htm
o
zamrażaniu
Podczas
demonstrowania zachowania tych bardzo zimnych cieczy trzeba zachować
elementarne zasady ostrożności. O ile dłoń (odwróconą wypukłością do góry) można bezpiecznie
polać ciekłym azotem (zjawisko Leidenfrosta, izolacja warstewką gazu), to
dostanie się skroplonego azotu do buta lub rękawa koszuli - może spowodować
niebezpieczne odmrożenia. W tych warunkach łatwo można niechcący „docisnąć”
ciecz do powierzchni skóry.
Odrębnym problemem jest zamrażanie
żywych tkanek. Najważniejsze jest wykonanie zamrożenia tak szybko, aby woda
krzepła w lód bezpostaciowy. Daje się to wykonać tylko z najmniejszymi
organizmami lub pojedynczymi komórkami (nasienia). Zamrażanie dużych organizmów
jest powolne z powodu zarówno dużego ciepła krzepnięcia wody, jak i złego
przewodnictwa cieplnego. W rezultacie wewnętrzne głębsze warstwy ciała są ochładzane powoli, a lód krzepnie w postaci wydłużonych kryształów,
które przebijają ścianki komórkowe i uszkadzają struktury komórek. Tak więc
ci, którzy nakazali (i opłacili!) zamrożenie swoich ciał po śmierci, nie
mają zbyt wielkich szans na powrót do życia (normalnego lub chociaż
jakiegokolwiek...) po rozmrożeniu w przyszłości. Klonowanie też tego nie
zapewni (chodzi przecież nie o ciało, a raczej osobowość, świadomość czy
duszę). Na razie pozostaje tylko forma trwałego zapisania się w pamięci
potomnych. (można zresztą zrobić to aż na dwa, diametralnie różne
sposoby...)
uzupełnienie
pokazów tlenu
W
uzupełnieniu opisów należałoby dodać demonstrację czerwonej
chemiluminescencji wzbudzonego tlenu gazowego w stanie singletowym (można
wykonać to nadspodziewanie prosto w zaciemnionej sali). A również
niezwykłą historię powstania obecnego, wtórnego składu atmosfery ziemi (to
bodaj jedyny przypadek tak wielkiej zawartości tlenu, w znanej nam części
Kosmosu). Oraz dramatyczną walkę naszego organizmu z uszkodzeniami
powodowanymi przez agresywne właściwości tlenu i produktów jego częściowej
redukcji; a więc demonstrację działania katalazy i peroksydazy.
Taki wykład o tlenie może być jednym z bardziej fascynujących...
Do
zilustrowania opisu musiałem z konieczności posłużyć się tylko
rysunkami... Na pewno bardziej atrakcyjne byłoby załączenie animowanego
filmu - tak jak w poniższych linkach.
LITERATURA
http://www.wsip.com.pl/serwisy/czaschem/c001olsz.html
[Karol Stanisław Olszewski]
http://www.seilnacht.tuttlingen.com/Lexikon/6Sauerst.htm
[leksykon: tlen]
http://www.allatoms.com/LOXpage.htm
[eksperymenty z ciekłym tlenem]
http://www.spusd.k12.ca.us/chemmybear/liqo2.html
[eksperymenty z ciekłym tlenem] strona nieczynna
http://www.physlink.com/Education/AskExperts/ae493.cfm
[przyczyna paramagnetyzmu tlenu]
http://www.enes.com.pl/index.htm
[oferta handlowa magnesów]
http://www.wondermagnet.com/main.shtml
[strona o silnych magnesach]
http://demoroom.physics.ncsu.edu/html/demos/188.html
[demonstracja paramagnetyzmu ciekłego tlenu
- film]
http://physics.kenyon.edu/coolphys/FranklinMiller/protected/Paramag.html
[jeszcze jeden film...]
http://www.pc.chemie.uni-siegen.de/pci/versuche/english/v85-4.html
[spalanie papierosa z ciekłym tlenem]
http://www.uh.edu/admin/srmd/labexplosion.html
[opis wypadków z ciekłym tlenem]
http://www.chem.leeds.ac.uk/delights/texts/expt_27.html
[świecenie wzbudzonego tlenu] http://science.ksc.nasa.gov/shuttle/technology/sts-newsref/et.html
[opis elementów budowy STS]
G.Bartosz.
"Druga twarz tlenu". PWN, Warszawa 1995.
J.Chem.Educ. 70,
613 (1993). [dlaczego
woda jest niebieska]
M.Ninnaert.
"Światło i barwa w przyrodzie". s. 328. Bibl. Problemów, WNT, Warszawa 1961.
R.P.Feynman,
R.B.Leighton, M.Sands. "Feynmana wykłady z fizyki", tom.1, cz.2. s. 100. WNT,
Warszawa 1963. [niebieskie niebo]
Tomasz Pluciński
nowy adres:
tomasz.plucinski@ug.edu.pl
 interesujących substancji. Ponieważ jednak powoduje
to odwieczny problem dydaktyczny: która temperatura jest wyższa: -183 o
C czy -196 o C, zatem proponuję posłużenie się osią liczbową.
Dodatkowo będzie widoczne, że skoro temperatura otoczenia jest o ok. 200 o
C wyższa od temperatury wrzenia ciekłego powietrza, to ciecz ta stale wrze.
interesujących substancji. Ponieważ jednak powoduje
to odwieczny problem dydaktyczny: która temperatura jest wyższa: -183 o
C czy -196 o C, zatem proponuję posłużenie się osią liczbową.
Dodatkowo będzie widoczne, że skoro temperatura otoczenia jest o ok. 200 o
C wyższa od temperatury wrzenia ciekłego powietrza, to ciecz ta stale wrze.


